Анилин и его свойства и противопоказания
 История анилина началась в XIX веке. Сегодня продукция, изготовленная на его основе, прочно вошла в повседневный обиход. За это время учёные, эксперты производства всесторонне изучили свойства популярного реагента. Анилин (аминобензол, фениламин) является сильнодействующим ядом. Попадая в организм человека, он парализует систему доставки кислорода к тканям.
История анилина началась в XIX веке. Сегодня продукция, изготовленная на его основе, прочно вошла в повседневный обиход. За это время учёные, эксперты производства всесторонне изучили свойства популярного реагента. Анилин (аминобензол, фениламин) является сильнодействующим ядом. Попадая в организм человека, он парализует систему доставки кислорода к тканям.
Давайте выясним, что такое анилин, историю его открытия, физические и химические свойства, где он сейчас применяется, какие симптомы указывают на острое и хроническое отравление им, о последствия интоксикации и мерах профилактики.
Что такое анилин
Это органическое соединение, которое относится к классу ароматических аминов. Впервые получил анилин немецкий химик Отто Унфердорбен в 1826 году, дав ему название кристаллин. Но на этом его история открытия не закончилась. На протяжении следующих 17 лет во время исследований разных учёных его получали ещё трижды.
- В 1834 г. немецкий химик-органик Фридлиб Фердинанд Рунгe выявил анилин в каменноугольной смоле, дав ему название кианол.
- В 1840 г. немецко-русский химик Юлий Фёдорович Фрицше получил это вещество путём нагревания индиго с раствором гидроксида калия, назвав его анилином.
- В 1842 г. русский химик-органик Николай Николаевич Зинин синтезировал анилин путём восстановления нитробензола действием сульфида аммония, назвав его бензидамом.
И лишь в 1843 г. немецкий химик-органик Август Вильгельм Гофман установил общность этих соединений, названных разными именами.
Способы получения
Основной способ синтеза анилина — восстановление нитробензола. Сегодня в качестве восстановителя обычно применяют водород. Это самый распространённый промышленный метод получения анилина.
Часть производственных процессов позволяет использовать в роли восстановителей другие вещества — металлы (железо, цинк, олово), соли (хлорид олова, сульфиды щелочных металлов), сероводород. Успешно применяются в производстве каталитический и электрохимический методы восстановления.
Физические и химические свойства
Формула анилина — C6H5NH2 содержит аминогруппу, поэтому вещество имеет второе название — фениламин. А также благодаря присутствию бензольной группы, он известен как аминобензол.
По своим физическим свойствам анилин — это бесцветная маслянистая жидкость, малорастворимая в воде. Имеет неприятный аммиачный запах. При горении образует яркое коптящее пламя. Температура кипения анилина составляет 184,4 °C. Это горючее вещество — при нагревании выше 70 °C могут образоваться взрывоопасные соединения. На воздухе анилин легко окисляется и приобретает красно-бурый цвет.
Благодаря химическим свойствам взаимодействует с сильными неорганическими кислотами (соляная, серная, фосфорная) и образует соли.
Применение
Анилин — это одно из первых органических соединений, полученных искусственным путём. Его открытие привело к созданию нескольких успешных отраслей.
В промышленности
Производственное использование анилина охватывает различные области — от получения ракетного топлива до изготовления крема для обуви.
Анилин и его соединения применяют в производстве:
- полиуретанов (конструкционные материалы, тепло- и звукоизоляция);
- ускорителей для вулканизации на основе натурального и синтетических каучуков (шины, резинотехнические изделия, резиновая обувь);
- красителей для тканей;
- эпоксидных полимеров;
- взрывчатых веществ;
- ингибиторов коррозии металлов;
- моторного топлива;
- смол, лаков.
Красители на основе анилина придают яркий цвет натуральным и синтетическим тканям, коже, шерсти, овчине. Однако существенным недостатком такого окрашивания является выгорание на солнце и низкая устойчивость к воздействию воды.
Анилин и его соединения являются сырьём для изготовления сложных промежуточных продуктов. Кроме основных областей применения, анилин используют при производстве гербицидов, пестицидов, фунгицидов, типографской краски, чернил, реактивов для фотографии, духов.
В медицине
Анилин является сырьём для фармакологической промышленности. Лекарства, изготовленные с его применением, оказывают следующее действие:
- обезболивающее, жаропонижающее — анальгин, бутадион;
- антимикробное — этазол, сульфален, сульгин, сульфаниламид, бисептол;
- нейролептическое — аминазин, пропазин.
Производные анилина входят в состав медицинских красителей. Метиленовый синий оказывает антисептическое, анальгезирующее действие. Генцианвиолет применяется как антибактериальное, противоглистное, местное противовоспалительное средство. Фуксин используют для местного лечения гнойничковых и грибковых заболеваний кожи, себореи. Красители применяют в бактериологических исследованиях для окраски микроорганизмов.
Действие на организм человека
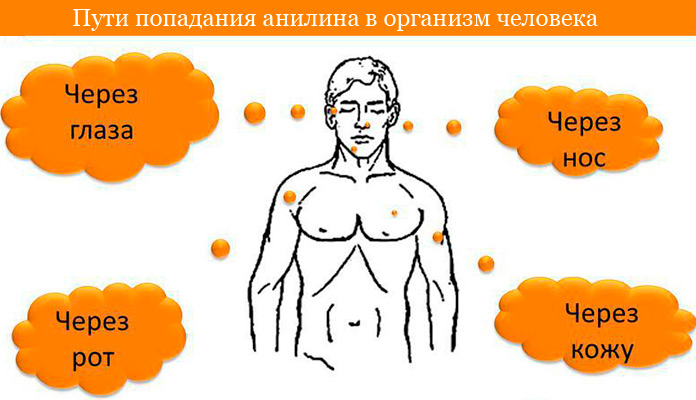
Анилин является сильным ядом, высокотоксичным для человека. Чаще всего интоксикация развивается при поступлении вещества через дыхательные пути, неповреждённую кожу и слизистые оболочки — ротовую полость, глаза. Небольшое количество может проникать через желудок.
Выводится вещество из организма в основном через почки. Оставшаяся часть выходит через дыхательные пути.
Анилин является гемотоксином, то есть наносящим вред крови человека. Механизм анилинового отравления состоит в образовании метгемоглобина, разрушении эритроцитов. Блокируется транспорт кислорода, что ведёт к поражению центральной нервной системы.
Кроме инактивации гемоглобина, токсичность анилина проявляется в развитии острой дыхательной, сердечно-сосудистой, почечной, печёночной недостаточности.
Накапливается анилин в печени и жировой ткани, создавая депо. Горячий душ, сауна, баня, приём алкоголя могут спровоцировать повторный выход токсина из депо в кровь, вызвав ухудшение состояния даже спустя две недели.

Отравление анилином
При кипении анилин образует пары, которые тяжелее воздуха. В производстве красителей, высока опасность отравления при соприкосновении с его растворами.
Причины отравления:
- непосредственный контакт с веществами в процессе их производства, хранения и применения;
- передозировка лекарственных препаратов;
- суицидальные попытки (нейролептиками);
- нарушения требований техники безопасности на производстве или в домашних условиях;
- аварии на промышленных объектах;
- загрязнение атмосферы ядовитыми парами, водоёмов стоками.
Отравление анилиновыми красителями может произойти в домашних условиях. Их используют для изменения цвета тканей, нанесения рисунков. Концентрация, состав красок рассчитаны на применение вне производственных объектов. Перед началом работы необходимо внимательно прочитать инструкцию. Соблюдение её пунктов обезопасит от случайной интоксикации.
Симптомы острого отравления
Степень тяжести состояния пострадавшего зависит от пути попадания вещества, его концентрации, исходного самочувствия человека. Клиника острого отравления анилином характерна для «яда крови».
Симптомы интоксикации лёгкой степени:

- жалобы на головную боль, слабость, недомогание, диспепсию в виде тошноты, рвоты;
- после приёма внутрь — боль в подложечной области;
- при осмотре выявляется синюшность губ, носогубного треугольника, ушных раковин, ногтей — акроцианоз.
Симптомы отравления средней степени:
- жалобы на сильную головную боль, тяжесть и болезненность в правом подреберье;
- изменения поведения — беспокойство, раздражительность, двигательное возбуждение;
- при осмотре — желтушность склер, выраженный акроцианоз;
- двигательные нарушения в виде неустойчивости при ходьбе;
- затруднение дыхания (одышка), усиленное отделение мокроты;
- учащение пульса.
Симптомы острого отравления анилином тяжёлой степени:
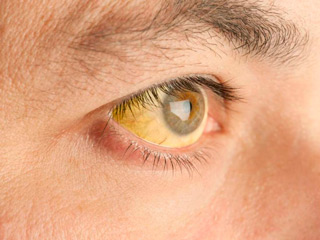
- синюшность кожного покрова, слизистых;
- желтушность кожи, склер;
- угнетение сознания до комы;
- развитие судорожного синдрома;
- одышка, учащение или урежение, патологический характер дыхательных движений (поверхностное, неритмичное);
- снижение артериального давления, учащение пульса, невозможность его определить на лучевой артерии;
- отсутствие мочеиспускания.
Синюшность при отравлении анилином имеет характерный оттенок. Его придаёт коричневый цвет метгемоглобина и красно-синеватый тон поражённого эритроцита. Кожа, губы приобретают сине-чёрный цвет.
На фоне нарастающей сердечно-сосудистой и дыхательной недостаточности наступает остановка кровообращения.
Симптомы хронического отравления
 Клинические проявления хронической интоксикации анилином развиваются постепенно и являются неспецифичными по своему характеру. Человека беспокоят головные боли, слабость, быстрое утомление, расстройства сна. Близкие, коллеги отмечают его возросшую раздражительность, снижение внимания, памяти. У пострадавшего наблюдаются симптомы поражения желудочно-кишечного тракта, печени, почек.
Клинические проявления хронической интоксикации анилином развиваются постепенно и являются неспецифичными по своему характеру. Человека беспокоят головные боли, слабость, быстрое утомление, расстройства сна. Близкие, коллеги отмечают его возросшую раздражительность, снижение внимания, памяти. У пострадавшего наблюдаются симптомы поражения желудочно-кишечного тракта, печени, почек.
Появляются шаткость походки, мышечные подёргивания. Характерны признаки расстройства зрительного аппарата — утомляемость глаз, светобоязнь, снижение остроты зрения. Возможно, образование сыпи на коже.
Симптомы не угрожают жизни, но при отсутствии лечения приводят к глубокой инвалидизации.
Первая помощь при остром отравлении
После прекращения вдыхания анилина или контакта с реагентами его содержащими, метгемоглобин в крови начинает распадаться. Восстанавливается транспорт кислорода к тканям, устраняется причина интоксикации.
При остром отравлении анилином, важна правильная последовательность оказания первой помощи. Её необходимо начинать с прекращения поступления яда в организм: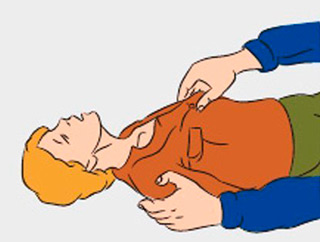
- устранить источник;
- проветрить помещение;
- снять загрязнённую одежду;
- если состояние пострадавшего позволяет — перенести его в безопасное место.
Мероприятия первой помощи при остром отравлении анилином:
- обратиться к медицинским специалистам (служба «скорой помощи», фельдшер здравпункта);
- промыть чистой водой глаза, прополоскать рот;
- при угнетении сознания нельзя поить, давать таблетки, пытаться промывать желудок;
- до приезда медицинских специалистов наблюдать за сознанием пострадавшего, его дыханием и частотой пульса;
- при развитии терминального состояния проводить сердечно-лёгочную реанимацию.
При суицидальных попытках с использованием нейролептиков, содержащих анилин, промывание желудка можно проводить только в случае ясного сознания и удовлетворительного состояния. То есть, практически сразу после приёма препаратов. При их всасывании снижается артериальное давление, угнетается кашлевой рефлекс, сознание. Манипуляция может осложниться аспирацией желудочного содержимого (затекание в дыхательные пути), развитием острой сердечной и сосудистой недостаточности.
Лечение
Диагностика отравления анилином проводится на основании сбора анамнеза, клинического обследования, результатов лабораторного и аппаратного исследования.
Кроме стандартных анализов, проверяют уровень фракции метгемоглобина (FMetHb) в сыворотке крови. Он присутствует в здоровом организме как продукт метаболизма, в количестве не более 1,0–1,5% от общего гемоглобина (Hb). При отравлениях симптомы появляются при значениях больше 3% FMetHb.
 Принципы лечения острого отравления анилином, следующие:
Принципы лечения острого отравления анилином, следующие:
- внутривенное введение антидота — метиленовый синий, аскорбиновая кислота, тиосульфат натрия;
- инфузионная терапия солевыми растворами;
- диуретики (мочегонные препараты);
- коррекция функции дыхания — в зависимости от показаний перевод на искусственную вентиляцию лёгких;
- методы эфферентной детоксикации — гемодиализ, гемосорбция;
- гипербарическая оксигенация для восстановления транспорта кислорода;
- мониторинг артериального давления, частоты сердечных сокращений, ЭКГ, температуры тела, диуреза, лабораторных анализов.
Интенсивная терапия проводится в условиях отделения анестезиологии-реанимации.
При подозрении на хроническое отравление анилином необходимо обратиться к врачу и пройти обследование. Анализы фракций гемоглобина доступны в амбулаторных условиях.
Последствия отравления
Интоксикация анилином опасна не только в острой, но и хронической форме. При длительном его воздействии на организм человека развиваются:
- осложнения со стороны центральной и периферической нервной системы, печени, почек, селезёнки, сердца, лёгких, желудочно-кишечного тракта;
- нарушения функций зрительного аппарата;
- дерматиты;
- анемия.
Канцерогенность анилина и его соединений для человека не доказана. Такие результаты получены только при исследованиях на лабораторных животных.
Симптомы анилиновой интоксикации неспецифичны. Избежать последствий хронического отравления поможет регулярное прохождение медицинских осмотров, предусмотренное федеральным законодательством.
Профилактика отравлений
Анилин относится к веществам II класса опасности — ГОСТ 12.1.005. Предельно допустимая концентрация (ПДК) в воздухе производственных помещений — 0,1 мг/м3.
Техника безопасности при работе с анилином предусматривает:

- использование средств индивидуальной защиты — костюма, перчаток, маски, очков;
- оборудование производственных помещений приточно-вытяжной вентиляцией;
- регулярное забор анализов воздуха в рабочих зонах;
- запрещение курения и питания в рабочих помещениях;
- соблюдение требований пожарной и взрывоопасности.
При сжигании анилина в воздух попадают токсичные или едкие пары — аммиак, оксиды азота, а также горючие пары, которые тоже могут вызвать отравление.
Работая в домашних условиях с анилиновыми красителями, необходимо следить за самочувствием. При появлении тревожных симптомов важно сразу же проветрить помещение или покинуть его.
Подводим итоги. Анилин — это органическое соединение, нашедшее применение в разных сферах промышленности. В лечебных дозах он входит в состав лекарственных препаратов. История использования анилина неразрывно связана с изучением признаков отравления этим сильнодействующим ядом. Чаще всего он попадает в организм через дыхательные пути. При своевременном прекращении контакта с токсином прогноз заболевания значительно улучшается. Избежать отравления можно, предприняв несложные меры безопасности.
Первая помощь при отравлении химическими веществами
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 2 декабря 2019;
проверки требуют 8 правок.
| Анилин | |||
|---|---|---|---|
| Традиционные названия | Аминобензол Анилин Бензоламин Фениламин< | ||
| Хим. формула | C6H5NH2 | ||
| Рац. формула | C6H7N | ||
| Состояние | бесцветная или желтоватая жидкость | ||
| Молярная масса | 93,1265 ± 0,0055 г/моль | ||
| Плотность | 1,0217 г/см³ | ||
| Поверхностное натяжение | 43,3 Н/м | ||
| Динамическая вязкость | 3,71 Па·с | ||
| Энергия ионизации | 7,7 ± 0,1 эВ[1] | ||
| Скорость звука в веществе | 1659 м/с | ||
| Температура | |||
| • плавления | −6,3 °C | ||
| • кипения | 184,13 °C | ||
| • вспышки | 158 ± 1 °F[1] и 76 °C | ||
| • самовоспламенения | 562 °C | ||
| Пределы взрываемости | 1,3 ± 0,1 об.%[1] | ||
| Критическая точка | |||
| • температура | 425,65 °C | ||
| • давление | 5,134 МПа | ||
| Критическая плотность | 0,314 см³/моль | ||
| Давление пара | 0,6 ± 0,1 мм рт.ст.[1] | ||
| Растворимость | |||
| • в воде | 3,6 г/100 мл | ||
| • в циклогексане | 66,7 (30,8°C) | ||
| Диэлектрическая проницаемость | 6,89 | ||
| Показатель преломления | 1,5863 | ||
| Дипольный момент | 1,53 Д | ||
| Рег. номер CAS | 62-53-3 | ||
| PubChem | 6115 | ||
| Рег. номер EINECS | 200-539-3 | ||
| SMILES | NC1=CC=CC=C1 | ||
| InChI | 1S/C6H7N/c7-6-4-2-1-3-5-6/h1-5H,7H2 PAYRUJLWNCNPSJ-UHFFFAOYSA-N | ||
| RTECS | BW6650000 | ||
| ChEBI | 17296 | ||
| Номер ООН | 1547 | ||
| ChemSpider | 5889 | ||
| Предельная концентрация | 0,3 мг/м3 | ||
| ЛД50 | 9-12 мг/кг (кошки, внутрижелудочно), 132 мг/кг (мыши, внутрижелудочно) | ||
| Токсичность | Чрезвычайно токсичен для мелких млекопитающих, высокотоксичен для человека, является гематотоксином (вызывает гемолиз). | ||
| Пиктограммы ECB | |||
| NFPA 704 | 2 4 1 POI | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Анили́н (аминобензол, фениламин) — органическое соединение с формулой C6H5NH2, родоначальник класса ароматических аминов. Представляет собой бесцветную маслянистую жидкость с характерным запахом, немного плотнее воды и плохо в ней растворим, хорошо растворяется в органических растворителях. На воздухе быстро окисляется и приобретает красно-бурую окраску. Весьма токсичен. Название «анилин» происходит от названия одного из растений, содержащих индиго — Indigofera anil (современное международное название растения — Indigofera suffruticosa).
История[править | править код]
Впервые анилин был получен в 1826 году при перегонке индиго с известью немецким химиком Отто Унфердорбеном (нем. Otto Unverdorben), который дал ему название «кристаллин».
В 1834 году Фридлиб Фердинанд Рунгe обнаружил анилин в каменноугольной смоле и назвал «кианолом».
В 1840 году Юлий Фрицше получил анилин нагреванием индиго с раствором KOH и назвал его «анилином».
В 1842 году Николай Зинин получил анилин восстановлением нитробензола действием (NH4)2S и назвал его «бензидамом».
В 1843 году Август Вильгельм Гофман установил идентичность всех перечисленных соединений.
Промышленное производство фиолетового красителя мовеина на основе анилина началось в 1856 году.
Получение[править | править код]
В промышленности анилин получают в две стадии. На первой стадии бензол нитруется смесью концентрированной азотной и серной кислот при температуре 50—60 °C, в результате образуется нитробензол. На втором этапе нитробензол гидрируют при температуре 200—300 °C в присутствии катализаторов:
Впервые восстановление нитробензола было произведено с помощью железа:
Другим способом получение анилина является восстановление нитросоединений — реакция Зинина:
Также, в анилин — идёт восстановление нитробензола цинком в присутствии избытка соляной кислоты.
;
;
И этот избыток связывает образующийся анилин в соль под названием хлорид фениламмония (анилин солянокислый):
;
Эта соль легко растворима в образующейся при этом воде и может быть выкристаллизована из неё,
к тому же после обработки щелочью хлорид фениламмония — даёт анилин:
Химические свойства[править | править код]
Для анилина характерны реакции как по аминогруппе, так и по ароматическому кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов. С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению с алифатическими аминами и даже с аммиаком. С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол. Хорошо галогенируется, нитруется и сульфируется. Например, анилин энергично реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок). С HNO2 дает диазосоединения.
Окисление[править | править код]
В отличие от аминов алифатического ряда, ароматические амины легко окисляются. Примером может служить реакция хромовой смеси с анилином, в результате образуется краситель «чёрный анилин».
Классическая реакция окисления анилина дихроматом калия в кислой среде часто используется как качественная реакция на анилин:
Аналитическим эффектом в данном случае служит появление окраски раствора от тёмно-синей до чёрной. Как и в большинстве реакций окисления анилина, продуктами являются различные Хиноны.
Другой качественной реакцией на анилин, очень чувствительной, является окисление анилина хлорной известью, при котором появляется фиолетовое окрашивание[2].
Реакции электрофильного замещения[править | править код]
Аминогруппа, являясь заместителем первого рода, оказывает сильное активирующее влияние на бензольное кольцо, из-за чего при нитровании может произойти окисление молекулы анилина. Для предотвращения окисления аминогруппу перед нитрованием «защищают» ацилированием.
Реакции на азот[править | править код]
С азотистой кислотой образует катион диазония, например:
Эта реакция может быть использована для получения фенола, если вместо соляной кислоты использовать разбавленную серную:
Где сначала образуется та же диазониевая соль, которая при нагревании в разбавленном водном растворе гидролизуется и разлагается до фенола, при этом выделяется молекулярный азот.
В связи с нестойкостью азотистой кислоты её часто заменяют нитритом щёлочного металла в кислой среде. Диазониевые соли используют для реакции Зандмейера.
Другие реакции[править | править код]
Гидрирование анилина в присутствии никелевого катализатора даёт циклогексиламин.
Анилин взаимодействует с соляной кислотой с образованием хлорида фениламмония[3]:
Анилин взаимодействует с бромом и даже бромной водой с образованием 2,4,6-триброманилина[4]:
Производство и применение[править | править код]
Изначально анилин получали восстановлением нитробензола молекулярным водородом; практический выход анилина не превышал 15 %. При взаимодействии концентрированной соляной кислоты с железом выделялся атомарный водород, более химически активный по сравнению с молекулярным. Реакция Зинина является более эффективным методом получения анилина. В реакционную массу вливали нитробензол, который восстанавливается до анилина.
По состоянию на 2002 год, в мире основная часть производимого анилина используется для производства метилдиизоцианатов, используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуков, гербицидов и красителей (фиолетового красителя мовеина)[5].
В России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты), но в связи с ожидаемым ростом производства полиуретанов возможно значительное изменение картины в среднесрочной перспективе.
Биологические свойства[править | править код]
Анилин — высокотоксичное вещество. В больших концентрациях фениламин оказывает негативное воздействие на центральную нервную систему. Кровеносный яд, вызывает кислородное голодание организма за счёт образования в крови метгемоглобина, гемолиза и дегенеративных изменений эритроцитов.
В организм анилин проникает при дыхании, в виде паров, а также через кожу и слизистые оболочки. Всасывание через кожу усиливается при нагреве воздуха или приёме алкоголя.
При лёгком отравлении анилином наблюдаются слабость, головокружение, головная боль, синюшность губ, ушных раковин и ногтей. При отравлениях средней тяжести также наблюдаются тошнота, рвота, иногда, шатающаяся походка, учащение пульса. Тяжёлые случаи отравления аминобензолом крайне редки.
При хроническом отравлении анилином (анилизм) возникают токсический гепатит, а также нервно-психические нарушения, расстройство сна, снижение памяти и т. д.
При отравлении анилином необходимо прежде всего удаление пострадавшего из очага отравления, обмывание тёплой (но не горячей!) водой. Также применяют введение антидотов (метиленовая синь), сердечно-сосудистые средства или вдыхание карбогена. Пострадавшему надо обеспечить покой.
Предельно допустимая концентрация анилина в воздухе рабочей зоны 0,3мг/м3[6] по ГОСТ 12.1.005-76. В водоёмах (при их промышленном загрязнении) — ПДК 0,1 мг/л (100 мг/м3)[7].
В соответствии с ГОСТ 12.1.007-76 аминобензол относится ко II классу опасности[8].
Охрана труда[править | править код]
Порог восприятия запаха анилина человеком может быть, например, 0,37-2,82 мг/м3[9]; 3,8 мг/м3[10]. ПДК аминобензола в воздухе рабочей зоны[11] 0,3 мг/м3 (максимальная разовая) и 0,1 мг/м3 (средняя сменная за 8 часов). Применение широко распространённых фильтрующих СИЗОД в сочетании с «заменой фильтров по появлении запаха под маской» (как рекомендуется в РФ[12]) приведёт к запоздалой замене противогазных фильтров и чрезмерному воздействию анилина на, по крайней мере, часть работников. Для их защиты необходимо использовать значительно более эффективные изменение технологии и средства коллективной защиты.
Примечания[править | править код]
- ↑ 1 2 3 4 https://www.cdc.gov/niosh/npg/npgd0033.html
- ↑ Окисление анилина раствором хлорной извести. Единая коллекция цифровых образовательных ресурсов. Дата обращения 14 августа 2017.
- ↑ Цветков Л.А. § 36. Амины // Органическая химия. Учебник для 10 класса. — 20-е изд. — М.: Просвещение, 1981. — С. 171—175.
- ↑ Габриелян О.С. § 16. Амины. Анилин // Химия. 10 класс. Базовый уровень : учеб. для общеобразоват. учреждений. — 4-е изд. — М.: Дрофа, 2008. — С. 116—121.
- ↑ Aniline (англ.) (недоступная ссылка). www.the-innovation-group.com (19 February 2002). — Aniline producers price capacity market demand consumption production growth uses outlook n.d., The Chemical Market Reporter, Schnell Publishing Company. Дата обращения 14 августа 2017. Архивировано 19 февраля 2002 года.
- ↑ name=https://docs.cntd.ru_ГОСТ 313-77 Анилин технический. Технические условия (с Изменениями N 1, 2, 3)
- ↑ Анилин // Ангола — Барзас. — М. : Советская энциклопедия, 1970. — С. 32—33. — (Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров ; 1969—1978, т. 2).
- ↑ name=https://docs.cntd.ru_ГОСТ 5819-78 Реактивы. Анилин. Технические условия (с Изменениями N 1)
- ↑ Ткачев П.Г. Материалы к гигиенической характеристике анилина как загрязнителя атмосферного воздуха / Рязанов В.А., Гольдберг М.С. (ред). — Предельно допустимые концентрации атмосферных загрязнений. — Москва: Издательство «Медицина», 1964. — С. 41-58. — 204 с. — (Выпуск 8). — 2800 экз.
- ↑ Gregory Leonardos, David Kendall & Nancy Barnard. Odor Threshold Determinations of 53 Odorant Chemicals (англ.) // Air & Waste Management Association Journal of the Air & Waste Management Association. — Taylor & Francis, 1969. — February (vol. 19 (iss. 2). — P. 91-95. — ISSN 1096-2247. — doi:10.1080/00022470.1969.10466465.
- ↑ (Роспотребнадзор). № 54 // ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны» (рус.) / утверждены А.Ю. Поповой. — Москва, 2018. — С. 7. — 170 с. — (Санитарные правила).
- ↑ под ред. Сорокина Ю.Г., Преображенского В.Б. и др. 5. Сроки службы и признаки неисправности СИЗОД // Методические рекомендации по выбору и применению средств индивидуальной защиты органов дыхания (рус.). — Москва: Издательство «КОЛОС», 2006. — С. 22—35. — 56 с. — 2000 экз. — ISBN 5-10-003932-9.
Литература[править | править код]
- Артеменко А. И. Органическая химия. — М.: «Высшая школа», 1987. — 430 с.
Ссылки[править | править код]
- Анилин // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
