Гидридов свойства и противопоказания
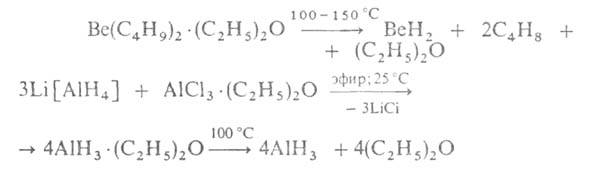
Каждый из нас сталкивался с понятиями такой науки, как химия. Иногда они так похожи, что трудно отличить одно от другого. Но очень важно разбираться во всех них потому, что иногда такое непонимание приводит к очень глупым ситуациям, а иногда и к непростительным ошибкам. В этой статье мы расскажем, что такое гидриды, какие из них опасны, а какие нет, где они применяются и как получаются. Но начнём с краткого экскурса в историю.

История
Свою историю гидриды начинают с открытия водорода. Этот элемент ещё в 18 веке нашел Генри Кавендиш. Водород, как известно, входит в состав воды и является основой всех остальных элементов таблицы Менделеева. Благодаря ему возможно существование органических соединений и жизни на нашей планете.
Кроме того, водород является основой и для многих неорганических соединений. В их числе кислоты и щёлочи, а также уникальные бинарные соединения водорода с другими элементами — гидриды. Дата их первого синтеза точно неизвестна, но гидриды неметаллов были известны человеку ещё с древности. Самый распространенный из них — вода. Да, вода — это гидрид кислорода.
Также к этому классу относят аммиак (основной компонент нашатырного спирта), сероводород, хлороводород и им подобные соединения. Более подробно о свойствах веществ из этого многообразного и удивительного класса соединений мы поговорим в следующем разделе.

Физические свойства
Гидриды — это в большинстве своём газы. Однако, если брать гидриды металлов (они неустойчивы в обычных условиях и очень быстро реагируют с водой), то это могут быть и твёрдые вещества. Некоторые из них (например, бромоводород) существуют и в жидком состоянии.
Дать общую характеристику такому огромному классу веществ просто невозможно, ведь они все различны и, в зависимости от элемента, входящего в состав гидрида, помимо водорода, имеют разные физические характеристики и химические свойства. Но их можно разделить по классам, соединения в которых чем-то схожи. Ниже рассмотрим отдельно каждый класс.
Ионные гидриды — это соединения водорода с щелочными или щёлочноземельными металлами. Они представляют собой вещества белого цвета, устойчивые при нормальных условиях. При нагревании эти соединения разлагаются на входящий в их состав металл и водород без плавления. Одно исключение — это LiH, который плавится без разложения и при сильном нагревании превращается в Li и H2.
Металлические гидриды — это соединения переходных металлов. Очень часто имеют переменный состав. Их можно представить как твёрдый раствор водорода в металле. Также имеют и кристаллическую структуру металла.
К ковалентным гидридам принадлежит как раз тот вид, что наиболее часто встречается на Земле: соединения водорода с неметаллами. Широкая область распространения этих веществ обусловлена их высокой устойчивостью, так как ковалентные связи являются самыми сильными из химических.
Как пример, формула гидрида кремния: SiH4. Если посмотреть на неё в объёме, то увидим, что водород очень плотно притянут к центральному атому кремния, а его электроны смещены к нему же. Кремний обладает достаточно большой электроотрицательностью, поэтому способен сильнее притягивать электроны к своему ядру, тем самым сокращая длину связи между ним и соседним атомом. А как известно, чем короче связь, тем она прочнее.
В следующем разделе обсудим, чем отличаются гидриды от других соединений в плане химической активности.

Химические свойства
В этом разделе также стоит поделить гидриды на те же группы, что и в прошлом. И начнём мы со свойств ионных гидридов. Их основное отличие от двух других видов в том, что они активно взаимодействуют с водой с образованием щёлочи и выделением водорода в виде газа. Реакция гидрид — вода довольно взрывоопасна, поэтому соединения чаще всего хранят без доступа влаги. Это делается потому, что вода, даже содержащаяся в воздухе, может инициировать опасное превращение.
Покажем уравнение вышеописанной реакции на примере такого вещества, как гидрид калия:
KH + H2O = KOH + H2
Как мы можем видеть, всё достаточно просто. Поэтому рассмотрим более интересные реакции, характерные для двух других видов описываемых нами веществ.
В принципе, остальные превращения, что мы не разобрали, характерны для всех типов веществ. Они склонны взаимодействовать с оксидами металлов, образуя металл, либо с водой, либо с гидроксидом (последнее характерно для щелочных и щёлочно-земельных металлов).
Ещё одна интересная реакция — термическое разложение. Оно происходит при высоких температурах и проходит до образования металла и водорода. Не будем останавливаться на этой реакции, так как уже разбирали её в предыдущих разделах.
Итак, мы рассмотрели свойства этого вида бинарных соединений. Теперь стоит поговорить об их получении.

Получение гидридов
Почти все ковалентные гидриды — это природные соединения. Они достаточно устойчивы, поэтому не распадаются под действием внешних сил. С ионными и металлическими гидридами всё чуть сложнее. Они не существуют в природе, поэтому их приходится синтезировать. Делается это очень просто: реакцией взаимодействия водорода и элемента, гидрид которого требуется получить.
Применение
Некоторые гидриды не имеют конкретного применения, но большинство — очень важные для промышленности вещества. Мы не будем вдаваться в подробности, ведь каждый слышал, что, например, аммиак применяется во многих сферах и служит незаменимым веществом для получения искусственных аминокислот и органических соединений. Применение многих гидридов ограничено особенностями их химических свойств. Поэтому их используют исключительно в лабораторных экспериментах.
Применение — слишком обширный раздел для этого класса веществ, поэтому мы ограничились общими фактами. В следующей части расскажем вам, как многие из нас, не имея должных знаний, путают безобидные (или по крайней мере известные) вещества между собой.

Некоторые заблуждения
Например, некоторые считают, что гидрид водорода — нечто опасное. Если и можно так называть это вещество, то никто так не делает. Если вдуматься, то гидрид водорода — это соединение водорода с водородом, а значит — молекула H2. Конечно, этот газ опасен, но только в смеси с кислородом. В чистом виде он не представляет опасности.
Существует много непонятных названий. Непривычного человека они повергают в ужас. Однако, как показывает практика, большинство из них неопасно и применяется в бытовых целях.
Заключение
Мир химии огромен, и, мы думаем, что если не после этой, то после нескольких других статей вы сами в этом убедитесь. Именно поэтому имеет смысл погружаться в его изучение с головой. Человечество открыло много нового, и ещё больше остаётся неизвестным. И если вам кажется, что в области гидридов нет ничего интересного, вы сильно заблуждаетесь.
ГИДРИДЫ, соединения водорода с металлами или менее электроотрицательными,
чем водород, неметаллами. Иногда к гидридам относят соед. всех хим. элементов
с водородом. Различают простые, или бинарные, гидриды, комплексные (см., напр.,
Алюмогидриды, Борогидриды металлов)и гидриды интерметаллич. соединений.
Для большинства переходных металлов известны также комплексные соед., содержащие
атом Н наряду с др. лигандами в координац. сфере металла-комплексообразователя.
Простые гидриды. Известны для всех элементов, кроме благородных
газов, платиновых металлов (исключение -Pd), Ag, Au, Cd, Hg, In, Tl. В
зависимости от природы связи элемента (Э) с водородом подразделяются на
ковалентные, ионные (солеобразные) и металлоподобные (металлические), однако
эта классификация условна, т. к. между разл. типами простых гидридов резких границ
нет.
К ковалентным относят гидриды неметаллов, Al, Be, Sn, Sb. Гидриды SiH4,
GeH4, SnH4, PH3, AsH3, SbH3,
H2S, H2Se, H2Te (см. табл. 1) и низшие
бороводороды-газы. Ковалентные гидриды обладают высокой реакц. способностью.
Эффективный положит. заряд атома Э в молекуле возрастает в пределах одной
группы периодич. системы с увеличением его порядкового номера. Элементы
Si и Ge образуют высшие гидриды общей ф-лы ЭnН2n+2 (п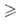 2),
2),
стабильность к-рых быстро уменьшается с увеличением числа атомов Э. Гидриды
элементов подгруппы S хорошо раств. в воде (р-ры имеют кислую р-цию), подгруппы
Р-незначительно. Гидриды элементов подгруппы Si взаимод. с водой с образованием
ЭО2 и Н2. Все эти гидриды раств. в неполярных или малополярных
орг. р-рителях. Ковалентные гидриды-сильные восстановители. Легко вступают в
обменные р-ции, напр. с галогенидами металлов. При 100-300 °С (H2S
ок. 400 °С) разлагаются практически необратимо до Э и Н2.
Табл. 1.-СВОЙСТВА ПРОСТЫХ КОВАЛЕНТНЫХ И ИОННЫХ ГИДРИДОВ
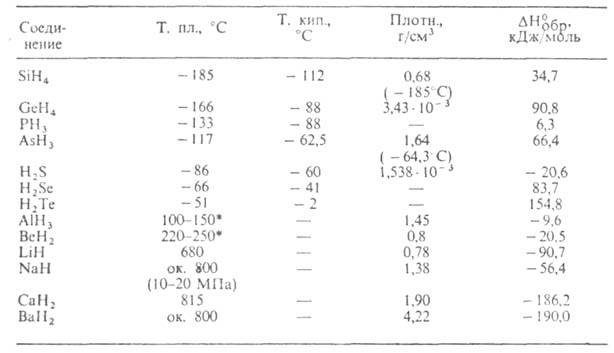
* Т-ра разложения.
Гидриды подгруппы фосфора получают р-цией ЭС13 с Li[AlH4]
в эфире при 25 °С; SiH4 и GeH4-взаимод. Мg2Э
с водой или с В2Н6 в жидком NH3; H2S,
H2Se и Н2Те-кислотным гидролизом сульфидов, селенидов
или теллуридов металлов (H2S-также взаимод. Н, и S). Все упомянутые
гидриды, особенно AsH3 и РН3, высокотоксичны. Гидриды
Ge, Si, As используют для получения полупроводниковых материалов. См. также
Мышьяка гидрид, Сероводород, Силаны, Фосфины.
Гидриды ВеН2 и А1Н3, существующие в полимерном
состоянии, а также крайне нестойкий термически Ga2H6
по природе хим. связи Э—Н близки к бороводородам: для них характерен дефицит
электронов, в связи с чем образование молекул или кристаллов происходит
с участием двухэлектронных трехцентровых мостиковых (Э—Н—Э) и многоцентровых
связей. Для этих гидридов характерны очень высокие энтальпии сгорания. Они взаимод.
с водой, выделяя Н2. С донорами электронов, напр. с NR3,
PR3, образуют аддукты, с В2Н6 в среде
апротонных орг. р-рителей-соотв. Аl[ВН4]3 и Ве[ВН4]2.
Получают гидриды Аl и Be по р-циям:
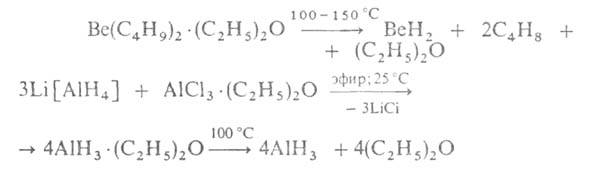
К ионным относят гидриды щелочных и щел.-зем. металлов (кроме Mg). Эти соед.-структурные
аналоги соответствующих галогенидов. Представляют собой кристаллы, к-рые
в расплавл. состоянии проводят электрич. ток, причем Н2 выделяется
на аноде. Не раств. в орг. р-рителях, хорошо раств. в расплавах галогенидов
щелочных металлов. Обладают высокой хим. активностью, бурно реагируют с
О2 и влагой воздуха. Взаимод. с водой (напр., МН + Н2О
-> МОН + Н2) сопровождается выделением тепла. В эфире, диглиме,
ТГФ легко (особенно LiH и NaH) реагируют с галогенидами или гидридами В
и А1, образуя соотв. борогидриды М[ВН4]n и алюмогидриды
М[А1Н4]n. При 700-800°С восстанавливают оксиды до
металлов. С СО2 дают соли муравьиной к-ты. Взаимод. с N2,
напр. 3СаН2 + + N2->Ca3N2 +
ЗН2.
Получают ионные гидриды обычно взаимод. Н2 с расплавом соответствующего
металла под давлением. Их используют в кач-ве сильных восстановителей (напр.,
для получения металлов из их оксидов или галогенидов, удаления окалины
с пов-стей изделий из стали и тугоплавких металлов). Многие гидриды-источники
Н2, перспективное ракетное топливо. Дейтериды и тритиегидриды
— возможное горючее для ядерных реакторов. См. также Лития гидрид.
Гидрид Mg по св-вам и природе хим. связи занимает промежут. положение
между ковалентными и ионными гидридами; кристаллы с решеткой типа ТiO2;
при высоких давлениях ( ~ 7 МПа) претерпевает полиморфные превращения.
С водой и водными р-рами к-т и щелочей MgH2 взаимод. с выделением
Н2, однако менее энергично, чем гидриды щелочных и др. щел.-зем.
металлов. М. б. получен взаимод. Mg с Н2 при 200-250 °С и давлении
10 МПа (скорость р-ции мала) либо обменной р-цией MgHal2 с МН
или М [А1Н4], где М—Li, Na, в среде орг. р-рителя. Легко образуется
при гидрировании сплавов Mg, содержащих небольшие добавки РЗЭ и переходных
металлов, при 150-180°С и 1-5 МПа, причем р-ция обратима. В связи с этим
такие сплавы-перспективные хим. аккумуляторы Н2 для нужд малой
энергетики, металлургии и хим. технологии.
К металлоподобным относят гидриды переходных металлов и РЗЭ. Формально такие
соед. могут рассматриваться как фазы внедрения водорода в металл. Их образованию
всегда предшествует адсорбция Н2 на пов-сти металла.
Адсорбированная молекула диссоциирует на атомы Н, в результате диффузии
к-рых в кристаллич. решетку происходит образование т.н.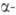 раствора
раствора
водорода в металле; процесс не сопровождается перестройкой кристаллич.
решетки. При достижении определенной концентрации Н2 в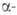 растворе
растворе
образуется собственно гидрид металла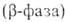
, как правило, стехиометрич. состава (МН3 для металлов III гр.,
МН2 для IV гр. и ванадия). Взаимод. Н2 с указанными
металлами (кроме Pd) всегда сопровождается перестройкой кристаллич. решетки.
Для описания природы хим. связи водорода с металлич. матрицей используют
представление о типе связи, промежуточном между ионной и металлической;
электроны водорода в большей или меньшей степени участвуют в формировании
зоны проводимости гидридов. По-видимому, вклад ионной составляющей связи М+
—Н- Наиб. велик для EuH2, YbH2 и тригидридов
лантаноидов и минимален для PdH0,6, а также для гидридов Mn,
Fe, Co, Ni, существующих при высоких давлениях Н2 и содержащих
менее одного атома Н на атом металла.
Металлоподобные гидриды (см. табл. 2)-светло- и темно-серые кристаллы с металлич.
блеском, устойчивые на воздухе при комнатной т-ре. С О2, водой
и водяным паром реагируют медленно. М.б. получены взаимод. металла с Н2
при обычной т-ре или при нагр.; напр., TiH2 и LaH3
синтезируют при 150-200 °С. Получение гидридов стехиометрич. состава в большинстве
случаев сопряжено со значит. трудностями из-за высокой чувствительности
гидрироваиия к наличию примесей в металле и особенно О2 и водяных
паров в Н2. Металлоподобные гидриды ограниченно применяют в кач-ве
источников Н2 высокой чистоты (используемых, напр., в топливных
элементах) и для поглощения Н2 из газовых смесей. Гидриды Pd-катализаторы
гидрирования, изомеризации, орто- и парапревращения Н2.
Табл. 2.-СВОЙСТВА МЕТАЛЛОПОДОБНЫХ ГИДРИДОВ
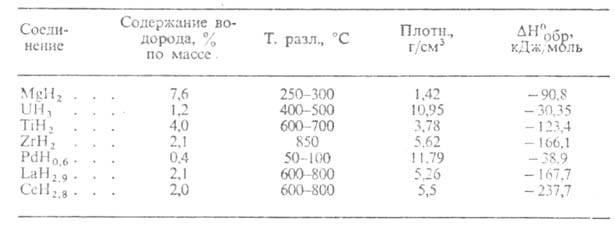
Гидриды интерметаллических соединений. Содержат обычно атомы
РЗЭ, Mg, Ca, Ti, Al, Fe, Co, Ni, Си. Легко образуются при взаимод. интерметаллидов
даже с техн. Н2 (содержащим до 1-2% примесей О2 и
водяного пара) при 25-200°С и давлениях Н2 0,1-1 МПа; скорость
поглощения Н2 очень велика. Р-ции характеризуются малыми тепловыми
эффектами (20-30 кДж на 1 моль Н2, для индивидуальных металлов-100-120
кДж) и не приводят к значит. изменениям в структуре исходной металлич.
матрицы; в большинстве случаев происходит лишь увеличение ее объема на
10-30%. Для гидридов этого типа характерна высокая подвижность водорода и большая
хим. активность (о св-вах см. также табл. 3).
При 200-500 °С и давлениях Н2 104-105
Па происходит гидрогенолиз интерметаллидов: мнх + м’ну
<- мм’n + н2 -> мнх + пМ’
Данная р-ция характерна для соед., образованных РЗЭ и Mg, а также РЗЭ
и Fe, Ni или Со. Так, гидрид РЗЭ, образующийся при гидрогенолизе интерметаллида,
содержащего Mg, катализирует как гидрирование Mg, так и дегидрирование
MgH2 при 150-180°С: МН2 + nMg + (n + 0,5) Н2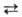
МН3 + nMgH2
Благодаря высокому содержанию Н2, возможности значит. смещения
равновесия в ту или др. сторону посредством небольших изменений т-ры и
давления Н2, способности поглощать Н2 при низких
т-рах и устойчивости к действию О2 и влаги воздуха, гидриды интерметаллич.
соединений м.б. использованы как хим. аккумуляторы слабосвязанного водорода.
Перспективно их применение как источников топлива для автономных энергосистем,
напр. автомобильного транспорта (см. Водородная энергетика), а также
для получения высокодисперсных металлич. порошков и катализаторов гетерог.
гидрирования.
Табл. 3.-СВОЙСТВА ГИДРИДОВ ИНТЕРМЕТАЛЛИЧЕСКИХ СОЕДИНЕНИЙ

===
Исп. литература для статьи «ГИДРИДЫ»: Гидриды металлов, пер. с англ., М., 1973; Девятых ГГ., Зорин А.
Д., Летучие неорганические гидриды особой чистоты, М., 1974; Антонова А.
М., Морозова Р. А., Препаративная химия гидридов. К., 1976; Водород в металлах,
пер. с англ., т. 2, М., 1981. К.Н. Семененко.
Страница «ГИДРИДЫ» подготовлена по материалам химической энциклопедии.

гидрид натрия неорганическое соединение формулы NaH. Он имеет ионную связь между натрием и гидридом. Его структура проиллюстрирована на рисунке 1. Он представляет собой солевой гидрид, что означает, что он представляет собой гидрид, подобный соли, состоящей из ионов Na + и H-, в отличие от более молекулярных гидридов, таких как боран, метан, аммиак. и вода.
Кристаллическая структура имеет координационное число 6, где каждая молекула натрия окружена 8 ионами гидрида, имеющими октаэдрическую форму, и показана на рисунке 2 (Марк Уинтер [Университет Шеффилда и WebElements Ltd, 1993-2016).
Соединение получают прямой реакцией между газообразным натрием и водородом (формула гидрида натрия — использование, свойства, структура и формула гидрида натрия, 2005-2017 гг.) Следующим образом:
H2 + 2Na → 2NaH
Гидрид натрия продается коммерчески в виде 60% мас. / Мас. Дисперсии (процентное отношение массы к массе) в минеральном масле для безопасного обращения (SODIUM HYDRIDE, s.f.).
индекс
- 1 Физико-химические свойства гидрида натрия
- 2 Реактивность и опасности
- 3 использования
- 4 Ссылки
Физико-химические свойства гидрида натрия
Гидрид натрия представляет собой белое твердое вещество в чистом виде, хотя обычно его получают в сером или серебристом цвете. Его внешний вид показан на рисунке 3.
NaH имеет молекулярную массу 23,99771 г / моль, плотность 1,396 г / мл и температуру плавления 800 ° C (Royal Society of Chemistry, 2015). Он нерастворим в аммиаке, бензоле, четыреххлористом углероде и сероуглероде (Национальный центр биотехнологической информации, s.f.).
Соединение крайне нестабильно. Чистый NaH может легко воспламениться в воздухе. Когда он вступает в контакт с водой, присутствующей в воздухе, он выделяет легковоспламеняющийся водород.
Когда он открыт для воздуха и влаги, NaH также легко гидролизуется в сильное коррозионное основание гидроксида натрия (NaOH) в соответствии с реакцией:
NaH + H2O → NaOH + H2
В этой реакции можно наблюдать, что гидрид натрия ведет себя как основание. Это связано с электроотрицательностью.
Натрий обладает значительно более низкой электроотрицательностью (≈1,0), чем водород (≈2,1), что означает, что водород извлекает электронную плотность по направлению к себе, удаляясь от натрия, образуя катион натрия и анион гидрида.
Чтобы соединение было кислотой Бренстеда, оно должно отделять электронную плотность от водорода, то есть соединять его с электроотрицательным атомом, таким как кислород, фтор, азот и т. Д. Только тогда он может быть формально описан как H + и может быть диссоциирован как таковой..
Гидрид намного лучше описан как H- и имеет свободную пару электронов. Таким образом, это основание Бренстеда, а не кислота. Фактически, если вы расширите определение кислоты / основания Бренстеда так же, как это сделал Льюис, вы придете к выводу, что натрий (Na +) является кислотным видом здесь..
Продукт реакции кислоты Бренстеда с кислотой-основанием H-основания и H + кислоты превращается в H2. Поскольку кислотный водород извлекается непосредственно из воды, газообразный водород может пузыриться, смещая равновесие, даже если реакция не термодинамически благоприятна.
Можно оставить ионы ОН-, которые можно записать вместе с остальной частью катиона Na +, чтобы получить гидроксид натрия (почему на основе твердого гидрида натрия, а не кислоты при реакции с водой?, 2016).
Реактивность и опасности
Соединение является мощным восстановителем. Атакует SiO2 в стекле. Воспламеняется при контакте с газообразными F2, Cl2, Br2 и I2 (последний при температуре выше 100 ° C), особенно в присутствии влаги, с образованием HF, HCl, HBr и HI.
Реагирует с серой с образованием Na2S и H2S. Может вступать в реакцию с диметилсульфоксидом. Активно реагирует с ацетиленом даже при -60 ° С. Самовоспламеняется во фторе.
Он инициирует реакцию полимеризации в этил-2,2,3-трифторпропионате, так что сложный эфир сильно разлагается. Присутствие в реакции диэтилсукцината и этилтрифторацетата, вызвало взрывы (SODIUM HYDRIDE, 2016).
Гидрид натрия считается разъедающим для кожи или глаз из-за потенциальных побочных продуктов едких реакций с водой.
В случае попадания в глаза их следует промыть большим количеством воды под веками не менее 15 минут и немедленно обратиться к врачу..
В случае попадания на кожу, немедленно почистите щеткой и промойте пораженный участок водой. Обратиться к врачу, если раздражение не проходит.
Это вредно при проглатывании из-за реакции на воду. Не вызывайте рвоту. Вам следует немедленно обратиться за медицинской помощью и перевести пострадавшего в медицинский центр..
Дисперсия гидрида натрия в масле не является пылью. Однако материал, который реагирует, может испускать мелкий едкий туман. При вдыхании прополощите рот водой и перенесите пострадавшего в место со свежим воздухом. Следует обратиться за медицинской помощью (Rhom and Hass Inc., 2007).
приложений
Основное использование гидрида натрия заключается в проведении реакций конденсации и алкилирования, которые развиваются в результате образования карбаниона (катализируемого основанием)..
Гидрид натрия в масле напоминает алкоголяты натрия и металла по своей способности действовать в качестве депротонирующего агента в эфире ацетоуксусной кислоты, Кляйзена, Стоббе, Дикмана и других связанных реакциях. Он имеет заметные преимущества перед другими конденсирующими агентами в том, что:
- Это более сильное основание, что приводит к более прямой депротонации.
- Нет необходимости в избытке.
- Произведенный H2 дает меру степени реакции.
- Вторичные реакции, такие как сокращения, устраняются.
Алкилирование ароматических и гетероциклических аминов, таких как 2-аминопиридин и фенотиазин, легко достигается с высоким выходом при использовании смесей толуол-метилформамид. Концентрация диметилформамида является переменной, используемой для контроля скорости реакции (HINCKLEY, 1957).
Было предложено использовать гидрид натрия для хранения водорода для использования в транспортных средствах на топливных элементах, причем гидрид заключен в пластиковые гранулы, которые измельчаются в присутствии воды для выделения водорода.
ссылки
- Хинкли, М. Д. (1957). Производство, обработка и использование гидрида натрия. Достижения в химии, том 19, 106-117.
- Марк Уинтер [Университет Шеффилда и WebElements Ltd, U. (1993-2016). Натрий: гидрид натрия. Получено с WebElements: webelements.com.
- Национальный центр биотехнологической информации. (Н.Д.). База данных PubChem Compound; CID = 24758. Получено из PubChem: pubchem.ncbi.nlm.nih.gov.
- Rhom and Hass inc. (2007 г., декабрь). Гидрид натрия 60% дисперсия в масле. Получено с сайта dow.com.
- Королевское химическое общество. (2015). Гидрид натрия. Получено от ChemSpider: chemspider.com.
- ГИДРИД НАТРИЯ. (2016). Получено из Cameochemicals: cameochemicals.noaa.gov.
- Формула гидрида натрия — Гидрид натрия. Использование, свойства, структура и формула. (2005-2017). Получено с Softschools.com: softschools.com.
- ГИДРИД НАТРИЯ. (Н.Д.). Получено из chemicalland21: chemicalland21.com.
- Почему на основе твердого гидрида натрия, а не кислоты при взаимодействии с водой? (2016, 20 апреля). Получено из stackexchange: chem.stackexchange.com.
